药事行政许可制度及对航空器适航审定的借鉴
摘要:我国药事行政许可制度实现了药品产销的各个阶段全程监督,注重维护行政相对人的权益,并且严格区分行政主体和行政相对人的法律责任。我国《适航管理条例》规定适航审定机关应当为其过失承担责任,该规定存在不周延性。应当由航空器的生产者和销售者承担产品责任;《适航管理条例》应明确适航审定机关的违法行为与损害后果之间的因果关系;要提升适航审定工作的持续性,完善相应的监督机制。
关键词:药事行政许可;航空器适航审定;行政责任
航空器适航安全审定作为一种行政许可,与其他类型行政许可有相似之处。药事领域行政许可与航空器适航审定都事关人民群众的生命安全。本文通过研究药事行政许可的运行机制,分析药事行政许可中的亮点,为航空器适航审定机制的完善提出建议。
一、药品审批程序及监督管理
药品审批流程涉及药品临床试验、检验、审评、审批等多个环节。探究行政主体在药品审批中的行政责任,首先需要厘清我国现行法律法规中药品审批的各项程序。药品审批过程中没有发现的安全性问题,在药品生产、销售、上市后评价时可能被发现。为了使药品质量安全得到充分保证,《药品管理法》和《药品注册管理办法》确立了若干监督管理程序。
(一)药品审批程序
1. 药品临床试验的审批程序
根据《中华人民共和国药品管理法》(以下简称《药品管理法》)的规定,药品申请上市注册前,须完成药品临床试验。国家药品监督管理局(以下简称“国家药监局”)是药品临床试验的审批部门。《药品管理法》第19条规定:“开展药物临床试验,应当按照国务院药品监督管理部门的规定如实报送研制方法、质量指标、药理及毒理试验结果等有关数据、资料和样品,经国务院药品监督管理部门批准。”与此同时,在药品临床试验审批之前,伦理委员会将审查药物临床试验是否符合伦理原则。[①]
2. 药品注册的审批程序
与药品临床试验类似,只有经过国家药监局批准,药品方可获得注册证书并上市。药品注册审批需要多个单位协同完成。根据《药品注册管理办法》第5条之规定,国家药监局依法组织药品注册、审评、审批以及相关的监督管理工作;国家药品监督管理局药品审评中心(以下简称“药品审评中心”)负责药物临床试验申请、药品上市许可申请的审评;中国食品药品检定研究院(以下简称“中检院”)承担创新药、改良型新药、生物制品以及其他药品的注册检验工作;[②]药典委核准药品通用名称;药品核查中心对申报资料的真实性、一致性以及药品上市商业化生产条件进行核查;药品评价中心进行非处方药适宜性审查。国家药监局、药品审评中心以及其他事业单位共同形成了三级药品审批机制(请见图1)。
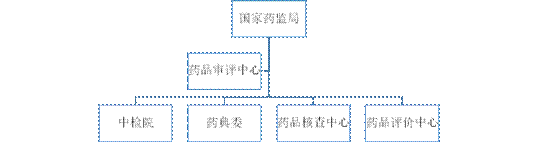
图1:三级药品审批机制
除了药品审评中心外,其他事业单位的工作对药品注册申请人能否注册成功会产生不同程度的影响。中检院、药典委、药品核查中心和药品评价中心的工作直接影响药品注册申请人的实体权利,特别是中检院,对药品能否被审批注册发挥着至关重要的作用。
3. 药品生产和经营的审批程序
在药品注册申请被批准后,药品上市许可持有人不可直接进行药品生产和销售,因为药品的生产和销售都必须分别获得药品生产许可证和药品经营许可证。生产、经营许可证由省、自治区、直辖区人民政府药品监督管理部门(以下简称“省级药监局”)审批。作为例外,新发现和从境外引进的药材,由国家药监局批准后,方可销售。[③]
(二)确保药品质量的监督管理程序
1. 药品注册审批完成前的监督管理程序
药品临床试验申请通过了国家药监局的审批之后,药品在临床试验过程中,仍然可能出现安全性问题。对于这种情况,临床试验申办者应当及时调整或终止临床试验;必要时,国家药监局可以责令调整或终止药物临床试验。[④]
在药品上市许可申请审评期间,如果发生可能影响药品安全性、有效性和质量可控性的重大变更的,药品注册申请人应当撤回原注册申请,补充研究后重新申报。[⑤]药品审评中心也可以基于存在的风险,决定是否开展药品注册研制现场核查。[⑥]
2. 药品通过注册审批后的监督管理程序
药品电子监管码可实现对药品生产、流通、消费的全程监管,维护药品生产商及消费者的合法权益。药品上市许可持有人、药品生产企业、药品经营企业和医疗机构应当建立并实施药品追溯制度,保证药品可追溯。[⑦]
药品上市许可持有人的法定代表人和主要负责人对药品质量全面负责。在药品的生产过程中,药品上市许可持有人有义务监督药品生产企业是否按照国家标准生产药品。不符合国家药品标准的,不得出厂。[⑧]
药品上市后,对药品的质量管理仍然不能放松。药品上市许可持有人、药品生产企业、药品经营企业和医疗机构应当经常考察药品质量、疗效和不良反应。如果发现疑似不良反应,应当及时报告。药品注册的有效期届满前,药品上市许可持有人需要申请再注册。上市评价后,如果药品疗效不确切、不良反应大或者因其他原因危害人体健康的,不予再注册。[⑨]
二、药品审批中行政责任
药品监管贯穿药品审批的全过程,而如果没有合适法律责任进行制约,那么药品监管就难以落实。在药品审批过程中,行政主体在决定药品能否上市、生产和销售的过程中发挥着重要作用,药品审批中的行政责任制度不能缺位。[⑩]行政责任主要包括行政处分和行政赔偿。
(一)药品审批中的行政处分
《药品管理法》规定了一些涉及药品审批部门行政处分的条款。例如,《药品管理法》第147条表明,如果药品不符合条件而药监局批准药品临床试验、颁发药品合格证书、颁发药品生产、经营许可证或医疗机构制剂许可证,主管人员则应当受到行政处分。如果药监局没有及时对发现的药品违法行为进行查处,或者未发现药品安全系统性风险,主管人员亦应受到行政处分。《药品管理法》第138条规定:“药品检验机构出具虚假检验报告的,责令改正,给予警告,对单位并处二十万元以上一百万元以下的罚款;对直接负责的主管人员和其他直接责任人员依法给予降级、撤职、开除处分,没收违法所得,并处五万元以下的罚款;情节严重的,撤销其检验资格。”
这些行政处分的共同特点在于,都以行政主体的行为存在过错为基础。如果因为科学技术水平有限而无法发现药品存在的问题,主管人员已尽合理义务进行审查,则不应受到处分。这类规则符合行政处分的构成要件,即行为人主观上必须有过错。[11]这也是行政处分区别于民事责任的重要方面。2005年卫生部印发的《卫生行政执法责任制若干规定》规定了过错责任追究制度。各级执法人员在执法活动中,因故意或重大过失导致特定情形发生的,应当承担相应责任。[12]
(二)药品审批中的行政赔偿
与行政处分不同,国家赔偿中的行政赔偿不以赔偿义务机关存在过错为前提。即使赔偿义务机关不存在过错,但是对自然人、法人和其他组织造成了损害,法律规定应当赔偿的,仍然须承担赔偿责任。
药品审批中的行政赔偿依托于现行法律的有关规定。在实践中,药品安全事故可能产生较为严重的损害,因而可能出现赔偿义务人无法负担赔偿的情形。如果行政主体在药品审批过程中存在不当行为,那么是否要承担连带赔偿责任或补充赔偿责任?药品审批中行政主体承担的赔偿责任是国家赔偿中的行政赔偿,与药品上市许可持有人承担的民事赔偿具有本质差异。在行政赔偿中,应当坚持赔偿法定原则,不能因为行政主体存在过错就认定行政主体应当与民事主体承担连带或按份责任。《国家赔偿法》列举了国家应当承担赔偿责任的情形,其中包括“其他造成财产损害的情形”。《药品管理法》第138条规定,如果药品检定机构出具的检验结果不实,造成损害的,应当承担赔偿责任。因此,药品检定机构出具不实检验报告,应当依法作出行政赔偿。与此同时,《药品管理法实施条例》第67条规定,药品监督管理部门及其工作人员违反规定,泄露生产者、销售者为获得许可而未经披露的数据,造成申请人损失的,药品监督管理部门应当承担赔偿责任,并可依法向故意或重大过失的工作人员追偿并给予行政处分。该条同时规定了行政赔偿和行政处分事项,突出了单位主体责任和向具体的个人进行追偿的制度。
如果根据相关法律法规授权,事业单位(包括技术检验、鉴定机构)也可能成为行政主体。[13]《药品管理法》特别授权了药品检验机构——中检院以检定药品的权力。药品检定机构应申请人请求对药品进行检定,检定结果与药品注册密切相关,检定过程不可豁免。因此,中国药品检定研究院处理药品检定事务并出具报告,是一种具体行政行为,应当受到行政法的规制,在满足一定条件下应当依法承担行政赔偿。
除了药品检定机构出具不实检验报告、药品监督管理部门违规泄露数据而应当承担赔偿责任之外,相关法律法规并没有规定其他应当承担国家赔偿的情形。特别是相关法律没有规定药监局、药品审评中心等机构在审批、审评确有错误并造成损失的情况下应当承担法律责任。这也体现出药品安全的首要负责人是药品上市许可持有人的法定代表人,[14]而不是承担药品审批职责的行政主体。
三、药品审批工作中的亮点以及对适航审定的借鉴
尽管在药品审批领域,我国现行法律法规还存在一些不足之处,药品审批程序中仍然有诸多值得借鉴的部分。本文结合航空器适航审定的实际需求,分析药品审批工作中的亮点以及对适航审定的借鉴。
(一)药品审批工作中的亮点
1. 药品产销的各个阶段全程监督
尽管相关法律法规明确规定药品许可证持有人有义务确保药品安全,《药品管理法》仍然规定了药品生产、运输、销售等各个阶段的监督机制,以确保药品安全得到全方位的维护。《药品注册管理办法》第12条规定:“药品注册证书有效期为五年,药品注册证书有效期内持有人应当持续保证上市药品的安全性、有效性和质量可控性。”然而药品生产企业具有逐利性,仅依靠企业自律是显然不够的。《药品管理法》从主动申报和被动检查两个方面强化了对药品产销各阶段的监督。
主动申报和被动检查往往具有共存关系。例如,在药品临床试验中,如果发现安全性风险或者其他风险,临床试验申办者应当调整或终止药品临床试验,国家药监局也可以根据实际情况责令调整临床试验方案或终止药品临床试验。[15]再如,药品许可证持有人、药品生产企业和经营机构应当考察本单位生产经营的药品的质量和不良反应;发现疑似不良反应的,应及时向药监局和卫健委汇报;对于确认发生严重不良反应的药品,国家药监局或省级药监局应当根据实际情况采取停止生产、销售等措施。[16]这类规则明确了行政主体和行政相对人保持药品安全的义务,避免出现推脱责任的情况。
《药品管理法》确立了全程可追溯、公开透明的药品监管制度。《药品管理法》第36条规定:“药品上市许可持有人、药品生产企业、药品经营企业和医疗机构应当建立并实施药品追溯制度,按照规定提供追溯信息,保证药品可追溯”。该规定充分落实了药品安全主体责任,确保每个环节的药品监管落到实处。该法第107条还确立了国家药品安全信息统一公布制度,要求全面、准确地公布国家药品安全总体情况、风险警示信息、重大药品安全事件及调查处理信息,使公众能够有效监督药品安全管理。
2. 药品审批中注重维护行政相对人的权益
药品审批的时间跨度较大,而研制创新药需要耗费巨大的成本,因而《药品管理法》注重维护行政相对人的权益。药品审批过程中,药品审批申请人可以查看相关审评审批的进度,能够及时跟踪相关审批情况。《药品管理法》体现了对行政权力的制约,避免药品审批久拖不决。例如,开展药物临床试验,国家药监局应当自受理临床试验申请之日起60个工作日内决定是否同意并通知临床试验申办者,逾期未通知的,视为同意。[17]《药品管理法》还规定行政主体应当与行政相对人及时进行沟通。如此处理,既提升了工作效率,又给行政相对人以补正材料的机会。例如,药典委在核查药品通用名称时,应当与申请人做好密切沟通,及时将结果通报申请人。
3. 严格区分行政主体和行政相对人的法律责任
在药品安全事故中,行政主体和新政相对人的法律责任的性质有所不同,《药品管理法》严格区分了这种差异。对于药品安全事故造成的民事赔偿责任,完全由药品行政许可持有人、药品生产者、药品销售者和医疗机构承担,行政主体不因审查不严格而承担连带责任或补充责任。从行政法学角度出发,行政主体只有在法律明确规定的情况下承担行政赔偿责任。从民法学角度出发,《中华人民共和国民法典》规定,由生产者和销售者承担因产品缺陷造成损害的赔偿责任,没有规定监管者应承担赔偿责任。因此,药监局不因审查疏忽导致药品流入市场而承担赔偿责任。行政主体只有在极少数情况下对药品行政许可申请人承担行政责任,如中检院出具的检验结果不实。这种严格区分行政责任与民事责任的方式,符合现行上位法的规定,有利于避免行政主体承担不必要的赔偿责任。
(二)我国现行适航审定责任机制及存在的问题
《芝加哥公约》附件8规定了航空器适航审定的若干标准。根据《芝加哥公约》第38条之规定,如果缔约国制定的适航审定标准与该标准存在差异,缔约国应通知国际民航组织。《芝加哥公约》确定的航空器适航审定标准,需要各国国内法予以落实,附件本身对适航审定申请人和主管机关不具有约束力,适航技术手册亦不能代替国内立法。英国司法实践关于民用航空器适航审定主要考察近因原则和勤勉义务。如果适航审定部门未尽勤勉义务,且航空器的缺陷与损害后果具有之间关联,那么适航审定部门应当承担赔偿责任。就我国而言,根据《中华人民共和国民用航空器适航管理条例》(以下简称《适航管理条例》)第24条之规定,民航局因适航管理工作的过失造成人身伤亡或重大财产损失的,应当承担赔偿责任,并对直接责任人员给予行政处分;构成犯罪的,依法追究刑事责任。这表明我国现行立法对航空器适航审定提出了较为严格的要求,适航审定机关在一定条件下须承担行政赔偿责任。
虽然《适航管理条例》规定适航审定机关应为其过失承担责任,但是该规定存在不周延性。其一,“造成人身伤害或财产损失”没有明确是导致适航审定申请人受到损害还是导致第三人(如乘坐航空器的旅客)受到损害,二者对因果关系的要求不同。其二,财产损害的赔偿条件之一为财产损害必须重大,其理论依据不足,因为在赔偿条件上区分轻微损害和重大损害,缺乏民法或行政法方面的依据。其三,欠缺赔偿责任限额,如果认定事故中适航审定机关存在重大过失,那么民航局将有可能承担高额赔偿责任。
(三)药品审批对适航审定管理的借鉴
药事审批中有不少亮点值得适航审定借鉴。第一,建议落实航空器主体责任,应当由航空器的生产者和销售者承担产品责任。从产品责任法角度出发,对于缺陷产品,应当由产品生产者进行赔偿,或者由产品销售者先行垫付后追偿。从民事责任理论出发,除非极个别情况下存在例外,一般情况下适航审定申请人和适航审定机关直接不存在共谋关系,民航局不应承担连带责任。建议借鉴《药品管理法》的有关规定,在《适航管理条例》中明确规定由产品生产、销售主体承担因产品缺陷所导致的赔偿责任,民航局只有在出现欺诈故意的情况下才承担责任。
第二,为了与《国家赔偿法》等上位法的规则和精神保持一致,《适航管理条例》应明确适航审定机关的违法行为与损害后果的因果关系。《国家赔偿法》规定损害后果和违法行为应有直接因果关系,《药品管理法》遵循了这一理念。在《适航管理条例》中要强调这一因果关系,避免国家赔偿制度的滥用。在发生飞行事故的情况下,航空器适航审定机关的失职与事故发生之间往往存在较多介入因素,二者没有直接因果关系。存在直接因果关系的法律行为或事实行为通常发生在航空器适航审定机关和适航审定申请人之间,即行政主体和行政相对人之间,这才是《国家赔偿法》所调整的对象。
第三,提升适航审定工作的持续性,完善监督机制。《药品管理法》确立了全方位、多层次的药品质量监管制度,药品通过审批注册后并非一劳永逸,药品许可证持有人、药品生产者和销售者必须持续监测药品不良反应并履行报告义务;药监局也可以主动介入药品不良反应事件;主管部门以一定方式公布药品安全信息。这种主动申报和被动检查相结合的管理模式,辅之以药品安全信息公开制度,有力地提升了药品安全监管的有效性。航空器适航审定也应提升监管的持续性,要求适航证书持有人、航空器生产者、销售者和使用者在其工作职责范围内,如发现航空器存在安全隐患,应当及时报告;民航局也可以在航空器使用过程中对已经颁证的航空器进行检查,相关情况及时向社会公布。如此处理,有利于防患于未然,提升航空器适航审定工作的质量。(作者:濮云涛)
[①] 参见《药品管理法》第20条第1款。
[②] 参见《药品注册管理办法》第53条。
[③] 参见《药品管理法》第63条。
[④] 参见《药品管理法》第22条。
[⑤] 参见《药品注册管理办法》第40条第1款。
[⑥] 参见《药品注册管理办法》第46条。
[⑦] 参见《药品管理法》第36条。
[⑧] 参见《药品管理法》第47条第1款。
[⑨] 参见《药品注册管理办法》第84条。
[⑩] 本文所称的行政责任是指行政主体未恰当履行行政管理职责而应当承担的责任,不包括行政相对人承担的行政法律责任。
[11] 参见翟月玲:《行政责任法律规制研究》,中国社会科学出版社2014年版,第6页。
[12] 参见第20条,具体的情形包括:超越法定权限的;认定事实不清、证据不足的;适用法律、法规、规章错误的;违反法定程序的;处理结果显失公正的;依法应当作为而不作为的;滥用职权侵害公民、法人和其他组织的合法权益的;卫生行政执法责任制不落实,责任不清造成重大过失的;其它违法行为。
[13] 参见刘芊:《中国行政法》,中国法制出版社2016年版,第66页。
[14] 参见《药品管理法》第30条第3款。
[15] 参见《药品管理法》第22条。
[16] 参见《药品管理法》第81条。
[17] 参见《药品管理法》第19条。


